Lattasi Persistenza e Diabete di tipo 2: che correlazione esiste?
Il consumo di Latte nelle persone con Lattasi Non Persistenza è associato a minor rischio di Diabete di tipo 2
SOMMARIO USCITA 103:
- Latte, diabete di tipo 2 e microbiota intestinale: una questione di co-metabolismo
- Bifidobatteri e diabete
- Conclusioni
Le recentissime evidenze hanno finalmente fatto luce sull’interazione tra diversi tipi di enzima lattasi, consumo di latte ed equilibrio del microbiota intestinale.
Utilizzando studi di metagenomica fecale e metabolomica del sangue, un team di ricercatori di Harvard e dell’Einstein College di New York guidato dal dr Qibin Qi ha potuto caratterizzare la flora batterica intestinale associata al consumo di latte, classificandola in base al tipo di enzima prodotto dai diversi soggetti studiati.
I risultati di questa analisi sono stati poi ricollegati al rischio di Diabete di Tipo 2 mediante lo studio dei metaboliti plasmatici prodotti dalle diverse forme di enzima espresso dall’ospite e dalla flora del microbiota.
Nello studio sono stati coinvolti 16.415 adulti ispanici e latini di diversa provenienza, per i quali sono state raccolte informazioni dettagliate relative ad aspetti sociodemografici, di salute e di alimentazione. (4)
Latte, diabete di tipo 2 e microbiota intestinale: una questione di co-metabolismo
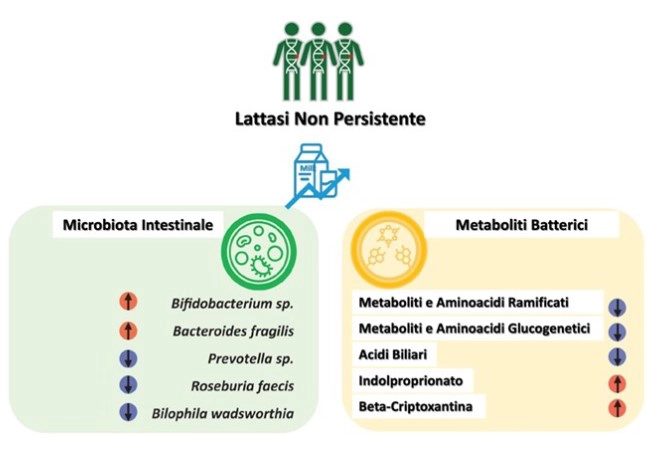
Grazie alle indagini del team del dr Qibin è stato possibile rilevare come tutte e sette le specie di Bifidobacterium particolarmente efficaci nel degradare il lattosio fossero abbondantemente presenti nel microbiota dei soggetti con Lattasi Non Persistente.
È interessante notare come i bifidobatteri siano microrganismi del microbiota particolarmente attivi nella metabolizzazione del lattosio (attraverso la produzione di specifiche lattasi batteriche), nella regolazione del sistema immunitario e del normale transito intestinale riducendo la produzione di gas ad opera di altri batteri fermentatori e migliorando, quindi, il quadro della intolleranza al lattosio. (9-12) Questo arricchimento, favorito dall’assunzione di latte, è inoltre accompagnato da una generale riduzione dei livelli di Aminoacidi Ramificati Glucogenetici insieme all’aumento dei livelli di Indolpropionato, che hanno dimostrato di essere associati alla riduzione del rischio di Diabete di Tipo 2. (13)
Al contempo, la condizione di Lattasi Non Persistente si associa ad una sensibile riduzione di microrganismi appartenenti al genere Prevotella, ampiamente rappresentati nel microbiota di pazienti affetti dal Diabete di Tipo 2, patologia per la quale tali batteri, unitamente ai metaboliti ad essi riconducibili, rappresentano un potenziale fattore di rischio per l’intolleranza al glucosio. (14)
Bifidobatteri e Diabete
Il Bifidobacterium sembra essere il genere più importante tra i microbi con potenziale ruolo protettivo contro il Diabete di Tipo 2. La quasi totalità della letteratura scientifica disponibile, infatti, riporta un’associazione negativa tra questo genere e il Diabete di Tipo 2, evidenziando la capacità di migliorare la tolleranza al glucosio. Alcune specie, in particolare, sono dotate di attività protettive peculiari:
- Bifidobacterium lactis: ha dimostrato di aumentare la sintesi del glicogeno e diminuire l’espressione dei geni correlati alla gluconeogenesi epatica, nonché di migliorare sia la traslocazione del trasportatore del glucosio-4 (GLUT4) e l’assorbimento del glucosio stimolato dall’insulina; (15)
- Bifidobacterium adolescentis: specie maggiormente efficace nell’alleviare i sintomi del Diabete di Tipo 2. Si tratta di un effetto strettamente correlato alla capacità di questi batteri di ripristinare l’omeostasi del microbiota intestinale, aumentando l’abbondanza di flora produttrice di acidi grassi a catena corta e alleviando l’infiammazione associata al Diabete di Tipo 2. (16)
Conclusioni
Lo studio del team di ricercatori guidato dal dr. Qibin sottolinea, ancora una volta, il prezioso ruolo del microbiota intestinale, responsabile non solo del mantenimento di una corretta funzionalità digestiva ma, in particolare, capace di attivare processi di co-metabolizzazione del lattosio assunto mediante il consumo di latte.
Il co-metabolismo del lattosio operato dagli enzimi lattasi della flora batterica caratterizzante i soggetti con Lattasi non Persistente che consumano latte, rappresenta, quindi, un vantaggio sia nella riduzione del rischio di sviluppare Diabete di Tipo 2 che in termini di sintomatologia dell’intolleranza stessa.
Va, infine, fatta una importante considerazione relativa alla conseguenza principale dell’intolleranza al lattosio, ovvero l’astensione dal consumo di latte e derivati da parte di chi ne soffre. Alla luce delle evidenze scientifiche più recenti emerge come, un consumo regolare di latticini da parte di soggetti con Lattasi Non Persistente, possa produrre ad una condizione di adattamento del colon derivante dalle importanti modifiche del microbioma intestinale prodotte da questi alimenti. Il lattosio, attraverso un potenziale effetto prebiotico selettivo, potrebbe infatti consentire alle persone con Lattasi Non Persistente di consumare latticini grazie al miglioramento sia della flora batterica intestinale che della sintomatologia derivante dall’intolleranza al lattosio. (17)
In un simile scenario, pertanto, anche i soggetti tipicamente intolleranti potrebbero non dover più rinunciare necessariamente alle virtù di un alimento prezioso come il latte, che nel contesto di una alimentazione adeguata ed equilibrata rappresenta un elemento protettivo aggiuntivo per malattie importanti quali, ad esempio, il Diabete di Tipo 2.
A cura della Redazione.
Bibliografia
1. Pereira, P. C. Milk nutritional composition and its role in human health. Nutrition 30, 619–627 (2014).
2. Gijsbers, L. et al. Consumption of dairy foods and diabetes incidence: a dose-response meta-analysis of observational studies. Am. J. Clin. Nutr. 103, 1111–1124 (2016).
3. Alvarez-Bueno, C. et al. Effects of milk and dairy product consumption on type 2 diabetes: overview of systematic reviews and meta-analyses. Adv. Nutr. 10, S154–S163 (2019)
4. Luo K, Chen GC, Kaplan RC, Qi Q, et al. Variant of the lactase LCT gene explains association between milk intake and incident type 2 diabetes. Nat Metab. 2024 Jan;6(1):169-186. doi: 10.1038/s42255-023-00961-1.
5. Itan Y, Jones BL, Ingram CJE, et al. A worldwide correlation of lactase persistence phenotype and genotypes. BMC Evol Biol. 2010 Feb 9:10:36. doi: 10.1186/1471-2148-10-36.
6. Segurel L, Bon C. On the evolution of lactase persistence in humans. Annu Rev. Genomics Hum. Genet. 18, 297–319 (2017).
7. Storhaug CL, Fosse SK, Fadnes LT, et al. Country, regional, and global estimates for lactose malabsorption in adults: a systematic review and meta-analysis. Lancet Gastroenterol. Hepatol. 2, 738–746 (2017).
8. Anguita-Ruiz A, Aguilera CM, Gil A. Genetics of lactose intolerance: an updated review and online interactive world maps of phenotype and genotype frequencies. Nutrients 12, 2689 (2020).
9. Reitmeier S. et al. Arrhythmic gut microbiome signatures predict risk of type 2 diabetes. Cell Host Microbe 28, 258–272 (2020).
10. Li, Q. et al. Implication of the gut microbiome composition of type 2 diabetic patients from northern China. Sci. Rep. 10, 5450 (2020).
11. He, Y. et al. Linking gut microbiota, metabolic syndrome and economic status based on a population-level analysis. Microbiome 6, 172 (2018).
12. JanssenDuijghuijsen L, Looijesteijn E, van den Belt M, et al. Changes in gut microbiota and lactose intolerance symptoms before and after daily lactose supplementation in individuals with the lactase nonpersistent genotype. Am J Clin Nutr. 2024 Mar;119(3):702-710. doi: 10.1016/j.ajcnut.2023.12.016. Epub 2023 Dec 28.
13. Qi, Q. et al. Host and gut microbial tryptophan metabolism and type 2 diabetes: an integrative analysis of host genetics, diet, gut microbiome and circulating metabolites in cohort studies. Gut 71, 1095–1105 (2022).
14. De Filippis F, Pasolli E, Tett A, et al.. Distinct Genetic and Functional Traits of Human Intestinal Prevotella copri Strains Are Associated with Different Habitual Diets. Cell Host Microbe. 2019 Mar 13;25(3):444-453.e3. doi: 10.1016/j.chom.2019.01.004.
15. Gurung M, Li Z, You H, et al. Role of gut microbiota in type 2 diabetes pathophysiology. EBioMedicine. 2020 Jan:51:102590. doi: 10.1016/j.ebiom.2019.11.051.
16. Qian X,Si Q, Lin G, et al. Bifidobacterium adolescentis Is Effective in Relieving Type 2 Diabetes and May Be Related to Its Dominant Core Genome and Gut Microbiota Modulation Capacity. Nutrients. 2022 Jun; 14(12): 2479. doi: 10.3390/nu14122479
17. Szilagyi A.Adaptation to Lactose in Lactase Non Persistent People: Effects on Intolerance and the Relationship between Dairy Food Consumption and Evalution of Diseases. Nutrients. 2015 Aug 13;7(8):6751-79. doi: 10.3390/nu7085309.